-
产品创新与产品经理务实(网课)
【课程概要】 企业的成功,与其产品的成功是分不开的。产品的成功意味着产品的战略/规划/开发/上市/退市等全生命周期管理的成功。但最终还是要靠人来落实,靠产品经理带领团队来实现产品的成功。 您或您的企业是否遇到: 1.产品不少,好卖的不多?立项需改进
-
产品线组织设计与运营
【课程概要】 企业发展在度过了早期创业的快速发展之后,随着组织规模的扩大和管理的复杂化,单项目管理的组织结构日益显得无法适应公司面向未来的发展战略要求,典型表现如下: 做正确的事与正确的做事的组织和职责没有分离。往往是正确的做事的组织(如产
-
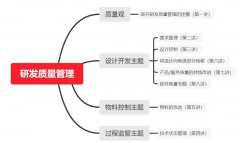
研发质量管理(网课)
研发质量管理(网课) 【课程概要】 PDCA戴明环在生产质量管理中得到了广泛的应用,取得了极为瞩目的成果,使产品从过去经常出现废品的报复演化到了谈论6西格玛的时代。但是PDCA用于研发质量管理却出现了许多困惑,生产质量管理专家拥有的生产质量管理经验到
-
战略解码与研发绩效管理操作实务
【课程背景】 管理的核心目标是提升绩效水平。企业竞争实力的提高,员工业绩水平的提高,需要职业化管理队伍素质的提高,需要各级主管绩效管理能力的提高。但是,很多企业的主管缺乏系统的绩效管理的理念、方法、工具和手段,对绩效管理的认识比较片面,绩效
-
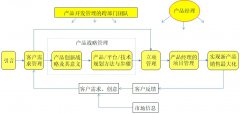
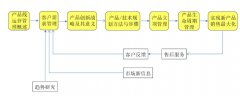
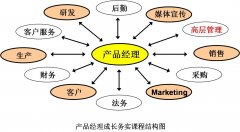
产品创新与产品经理务实
本课程将结合标杆企业在产品管理方面的最佳实践,一起探讨如何最大限度解决产品前端的模糊性,做正确的产品,上市就上量,保证开发出来的产品能够取得商业成功。(1)理解产品经理的定位、职责、素质及能力要求,与研发项目经理的区别以及组织运作的异同; (2)掌握客
-
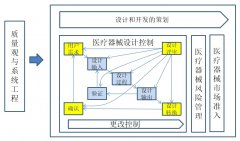
医疗器械系统工程最佳实践――MPI核心课程
【课程概要】 企业发展到一定规模,必然要划分出职能部门和进行专业分工。但是各职能部门人员往往更专注于各自专业领域,如软件、硬件、机械、电气等,互相之间交流和协作很少,协调配合就成为了突出问题,例如: 1)用户需求分析能力差,对产品应用场景缺乏
-
物料优选与可靠性管理(版权课)
■课程背景 据统计,用户投诉及生产过程中的不良大约有50%以上源自物料质量或使用问题。同时,原材料成本也在产品成本中占最大的比重。因此如何在保证物料质量同时降低成本,如何在质量和成本之间达到最优的平衡,是每一个制造型企业都要面临的问题。物料问
-
产品数据管理与流程优化
产品数据管理面对面─两天搞懂PLM 报名咨询:0755-26070628, 972843093@qq.com 本课程可为企业提供内训,欢迎来电咨询! 【课程背景】 产品开发是技术和管理结合成一体的复杂工程。产品数据繁多,研发项目管理活动与其相互关系极其复杂,这些
-
电子产品可测性设计(DFT)工程实践
随着电子信息产品,尤其是通讯产品日益激烈的市场竞争和产品的高密度、高集成度及高复杂度,如何能快速的、低成本的、高质量的向市场推出产品,是各企业必须面临的挑战。测试是产品质量保证的重要手段,如何快速、高效、低成本的完成产品的测试,缩短产品的稳
-
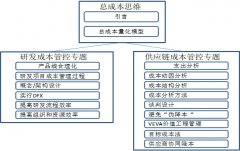
产品生命周期成本管理与降本修炼
【主办单位】 深圳市智杰科技信息有限公司 【报名咨询】0755-26070628,18038064508 【收费标准】4900元/1人/2天; (含两天中餐、指定教材、茶点、证书、税费等) 培训总学时为14小时,共2天。讲师团: 汪老师 , 项老师 本课程可为企业提供内训,欢迎来电咨
|返回首页|0755-26070628