我看迈瑞系统可靠性工程建设之路
浏览次数: 次
迈瑞作为医疗器械行业的一哥,迈瑞的系统可靠性工程实践被写入中国医疗器械行业白皮书,也为中国高端制造转型升级提供了可借鉴的范本。
本文作者作为迈瑞首任可靠性工作室负责人,深度引领和参与了迈瑞系统可靠性工程的建设,在此尽我所能为迈瑞系统可靠性工程的最佳实践作一个概略的描述,以帮助研发型企业提升质量与可靠性。
迈瑞的可靠性工程体系并非一蹴而就,而是通过“市场驱动+质量管理体系支撑+技术标准牵引+可靠性工程方法渗透”四位一体的方式,随着公司的发展逐步构建的。其核心逻辑在于:将可靠性作为产品竞争力的基石,通过系统工程方法将可靠性工程方法转化为研发过程中的技术和管理的体系能力。
1.迈瑞系统可靠性工程体系建立的核心背景与驱动力
1.1.行业要求
医疗设备直接关乎生命,对产品的安全性、有效性要求极高,而安全性就是特殊的可靠性。迈瑞需要满足全球不同市场(如FDA、CE、NMPA)严格法规和认证标准,市场环境倒逼迈瑞建立高标准的可靠性工程体系,以保障产品的安全性、有效性。
1.2.全球化竞争需求
进入国际市场后,迈瑞面临与GE、飞利浦、西门子等巨头的竞争,必须通过可靠性工程提升产品竞争力,打破国际市场对中国制造“低质低价”的刻板印象。
1.3.技术复杂、小批量多品种的挑战
随着新技术的应用,医疗器械智能化、集成化的发展,医疗器械的复杂度呈指数级增长,涉及专业包括软件、硬件、机械、光学、液气路、配方、临床、法规....等,技术涉及面广,同时又兼有小批量多品种的特点,产品开发团队普遍规模不大,每个专业方向往往是一个萝卜一个坑,这就使得产品开发团队面临着如何在有限资源条件下高效低成本地实施可靠性工程来规避潜在风险,从而应对保障产品安全性、有效性的挑战。
2.迈瑞系统可靠性工程体系建设成功的关键要素
2.1.最高管理者发挥领导作用
早在本世纪伊始,虽然迈瑞的现金流非常好,但是总裁李西廷却反复以韩国某监护仪品牌为例,该监护仪在全球急剧扩展市场份额,但是突发的安全性、有效性问题,使得该品牌迅速退出市场,销声匿迹。反躬自省,迈瑞的售后故障率偏高,日后会不会重蹈覆辙?不久后李西廷就提出设立可靠性工作室,对研发中心产品可靠性负责。最高管理者的忧患意识和实施可靠性工程的态度,是迈瑞系统可靠性工程建设成功的组织保障。
2.2.夯实质量管理体系作为系统可靠性工程的支撑框架
迈瑞的系统可靠性工程并不是独辟蹊径另搞一套,而是对质量管理体系的嫁接、延展、升级和强化。质量管理体系基础建设包括:
- 依据ISO 13485(医疗器械质量管理体系)、QSR、IVDR、MDR、GMP等国际国内标准,构建合规、高效的质量管理体系。
- 依据QSR820、IEC 62304等国际标准,构建以设计控制为核心的研发流程体系,涵盖了从策划到用户需求分析、设计输入、技术解决方案、设计输出、集成、设计转换、验证、确认、更改等产品开发生命周期中的所有的重要方面。
- 依据ISO 14971(风险管理)建立全生命周期的风险管理体系。
迈瑞的系统可靠性工程建设的理念并不去一定要区分什么是质量工作什么是可靠性工作,而是认为可靠性只不过是包含时间参数的产品质量,一切有效的产品质量措施都有助于提高可靠性。质量管理体系与可靠性工程中存在许多兼容性或协调性,应充分利用这些兼容性和协调性,如:
- 需求分析VS确定可靠性要求
- 项目策划VS确定可靠性工作项目
- 方案设计VS可靠性分析与设计
- 验证VS可靠性试验与评价
- 纠正预防措施(CAPA)VS故障报告纠正措施闭环(FRACAS)、可靠性增长
- 设计评审VS可靠性评审
- 风险管理VS失效模式效应分析(FMEA)、故障树分析(FTA)、使用可靠性评估与改进........等
将可靠性工程与质量管理体系相结合就是系统可靠性工程。实施系统可靠性工程就可以避免叠床架屋,简化管理,提高实施可靠性工程的效率。
迈瑞公司产品开发各阶段的可靠性工作如图1所示:
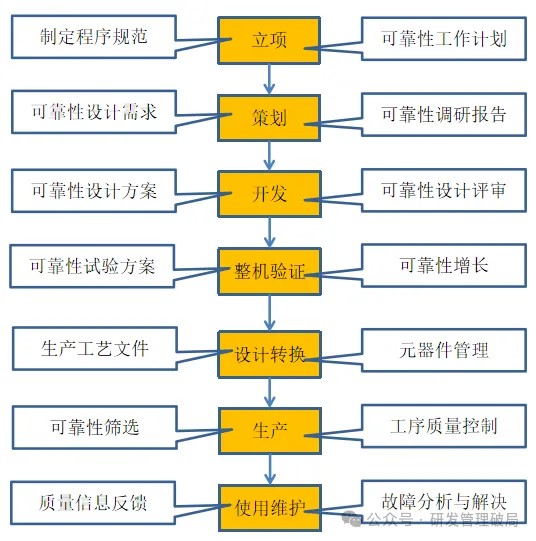
图 1迈瑞公司产品开发各阶段的可靠性工作
2.3.强化设计可靠性
迈瑞的可靠性分析与设计能力建设的起步是从满足适用技术标准要求开始的,包括各类通用安全标准和专用安全标准。包括了如下重要事项:
- 以各类通用安全标准为基础,结合产品开发经验教训形成通用设计指南;以专用安全标准为基础,结合产品开发经验教训形成型号设计指南。包括各个专业领域(光机电算配方液路等)和层级(整机、部件、零件、原材料等)。
- 建立了物料优选管理信息系统,使优选物料得以充分共享。
- 在研发阶段通过FMEA(失效模式与影响分析)、故障树分析(FTA)等工具识别潜在风险。
- 利用仿真技术(如热力学仿真、振动仿真)预测产品在极端环境下的表现,优化设计方案。
- 建立可靠性实验室,覆盖环境测试(高低温、湿度、盐雾)、机械测试(振动、冲击)、电气安全测试、EMC测试等,引入HALT(高加速寿命试验)和HASS(高加速应力筛选),通过极限条件暴露产品缺陷,缩短验证周期。
- 实验室专门建设了可靠性技术平台,包括案例分析、可靠性设计指南、培训课件、故障分析等模块以供查用,这对工程师提升可靠性设计(DFR)能力很有帮助。
- 开展可靠性合作:与电子五所、计量院、华测等达成的良好合作关系,解决了可靠性工作开展过程中面临着测试资源问题。与东芝医疗、DATASCOPE进行深度合作,快速获得了大量面向欧美市场进行产品开发的范式和经验。
2.4.建立生产可靠性
- 生产环境中引入了环境温湿度控制系统、静电防护系统、防尘措施,从而提高产品的可靠性。
- 在产品出厂前百分之百的产品都通过了高温老化及温度循环筛选等方式筛出了具有早期缺陷的产品,提前进入了失效率较低的偶然失效区,使出厂后的质量更为稳定,可靠程度更高。
- 物料认证及其管理:基础不牢地动山摇。物料问题引发的产品质量问题在电子设备中占很大比例,如何对物料实施有效认证和管理是迈瑞公司高度重视的问题。迈瑞公司成立专业部门,专门负责供应商选择、物料选型认证,从质量、成本、交付、服务等方面进行评估与验证,保证物料供应的质量与可靠性,使得物料质量与供应质量得到了持续改善。
- 供应商协同管理:对关键元器件供应商实施可靠性联合评审,建立长期合作的“零缺陷”供应链生态。
- 制造过程控制:通过数字化工厂(如MES系统)实现生产全流程可追溯,应用SPC(统计过程控制)确保工艺稳定性,采用PFMEA降低制造过程风险。
2.5.保障使用可靠性
考虑安装、操作、使用、维修保障等方面对产品可靠性的影响。包括采取如下措施:
- 通过调研从用户的角度编制使用说明书。
- 对客户进行产品知识、操作方法、使用维护培训。
- 售后服务工程师与客户建立密切联系,定期回访客户,进行设备维护并了解客户需求,通过各种方式提升服务质量,实际上也可以提高产品的使用可靠性。
- 将使用可靠性信息的收集、评估、改进,与欧盟关于医疗器械上市后的风险管理要求结合起来。
2.6.人员培养。
- 采取外部与内部培训相结合的方式开展不同层次、不同技术方向的培训和交流,力求把可靠性的理念、技术、方法贯彻到设计、生产和服务等环节当中,使得可靠性技术与专业技术方向实现了有效融合。
3.迈瑞系统可靠性工程体系建设历程简述
1995年
- TUVPS机构的ISO9001质量管理体系认证。
2000年
- 开展环境试验、EMC测试。
- 监护产品线编制良好设计指南,探索式使用。
- 通过了中国医疗器械质量认证中心CMDC的质量体系认证。
2002年
- 成立可靠性工作室,开始可靠性工程相关技术和管理的研究和推行。
- 与电子五所合作,彩超项目引入ESS(环境应力筛选试验)
- 正式编制和启用设计指南,纳入设计控制体系
- 开始建立物料优选清单,启动物料优选管理
- 开始在单板上试点实施可靠性评审,并逐步推广到其它组件和整机
- 引入DFMEA技术。在各技术方向。硬件、软件、液路等并行开展,并成立了DFMEA小组,已完成设计、分析、评审等一系列工作。
2003年
- 与东芝医疗合作的项目上,实施可靠性建模、可靠性预计、可靠性分配。
- 设计转换引入PFMEA
- 引入整机ESS(环境应力筛选试验)
- 引入电子设计仿真工具进行容差分析。
2004年
- 开始筹建专门的可靠性检测实验室,将委托外部测试逐渐变为自主测试,极大提高了可靠性设计的效率。包括三个专门的实验室。电磁兼容实验室、安全实验室和环境实验室。实验室严格按照国际实验室标准ISO17025要求制定质量运作体系。
- 引入蒙特卡诺仿真工具进行容差分析。
2007
- 实验室通过中国合格评定国家认可中心(CNAS)认可。
- 将ALT(加速寿命实验)开始引入产品开发阶段,用于帮助完成元器件的选型、可靠性指标测定等工作。
2008年
- 将(Halt)高加速寿命实验等可靠性实验方法引入产品开发阶段。
- 为每个产品线分派环境可靠性工程师。
2017
- 贯彻MDR、IVDR相关法规中有关安全性要求。
2019
- 贯彻唯一化标识(UDI)相关法规。
——至今
持续改进。
相关信息:IPD-ePACE咨询服务简介。

